Un biomédicament est un médicament issu de la biotechnologie, grâce à des organismes vivants « reprogrammés », comme l’insuline et les anticorps monoclonaux...
L’expiration des brevets des biomédicaments de référence déjà sortie en Europe ouvre la possibilité de produire et de commercialiser des médicaments similaires à ces derniers.
Pour obtenir son Autorisation de Mise sur le Marché (AMM), un médicament biosimilaire a fait la preuve de sa similarité biologique et clinique (qualité, sécurité, efficacité) avec le médicament de référence.
L’arrivée de ces médicaments biosimilaires sur le marché, notamment pour le traitement des maladies chroniques, et maintenant sur le champ de la cancérologie, représente un véritable enjeu de maîtrise des dépenses de santé pour maintenir un niveau élevé d’accès des patients à des traitements innovants.
Dans ce contexte, deux supports de communication sur les médicaments biosimilaires ont été élaborés par l’OMEDIT Nouvelle-Aquitaine avec le soutien de l’ARS et de l’Assurance
Maladie :
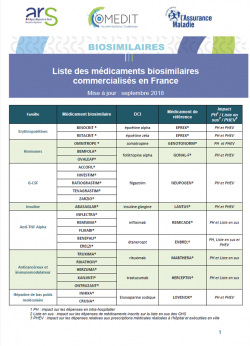
- « CONNAÎTRE LES MÉDICAMENTS BIOSIMILAIRES » (septembre 2018) : une version actualisée de la plaquette destinées aux professionnels de santé en ville ou à l’hôpital pour les informer su
- r les spécificités, sur la qualité et la sécurité des médicaments biosimilaires comprenant la liste des médicaments commercialisés en France.
- « LES MÉDICAMENTS BIOSIMILAIRES, C’EST QUOI ? » (septembre 2018) : une plaquette d’information destinée aux patients qui seraient concernés par une prescription de médicament biosimilaire (élaboré avec le soutien de l’URPS médecins libéraux, l’URPS pharmaciens et de France Asso Santé Nouvelle-Aquitaine)

Télécharger la « liste des médicaments biosimilaires commercialisés en France »
Lien vers les outils Omédit "médicaments biosimilaires"
Des formations spécifiques sur les médicaments biosimilaires sont organisées au deuxième semestre 2018 par l'Omédit Nouvelle-Aquitaine : lien vers le programme des formations et vers les formulaires d'inscription